 ノウキン
ノウキンどうも、しがない研究者『ノウキン』です。
今回も前回に引き続き『ハダカデバネズミ』を紹介します。
その名前と姿のインパクトが強烈な生物である『ハダカデバネズミ』。
ほとんど毛がなく出っ歯なその姿は、まさに「名は体を表す」を体現した生物ですね。


前回の記事では、そんなハダカデバネズミの生態を中心に解説しました。


アフリカのサバンナという過酷な環境で地下生活をしていることを知らなかった読者は意外と多いかもしれませんね。
また、ハダカデバネズミが哺乳類では超希少な『真社会性』を形成する生物であることも解説しました。
ハチやアリと同じ女王をトップとした階級社会を形成するのは驚きでしたよね。
上記のような特殊な生態が判明したことで、ハダカデバネズミは研究者達に注目され始めたのです。



ハチやアリと同じ『真社会性』を形成してるのは驚きました(汗)
そりゃ、研究者もハダカデバネズミを注目しますよね。



その後にもっと凄い発見があって、さらに注目されるんですけどね。





デバ吉!
ふとん係の仕事は終わったんですか?



とりあえず、他の仲間に任せてきました。
今回はハダカデバネズミの凄い特性について説明しますよ。



凄い特性…
一体どんな特性なんだろう?汗



具体的には『不老長寿』と『ガン化耐性』です。



…マジ?
初めは真社会性を形成する哺乳類として研究者達に注目されたハダカデバネズミ。
しかし、研究が進む過程でその驚異的な特性が判明しました。
その特性とは『不老長寿』と『ガン化耐性』。
今回はそんなハダカデバネズミの驚異的な2つの特性について解説します。
本記事ではハダカデバネズミの研究についての論文を参考文献にしています。
各章の最後に参考文献である論文のURLを載せますので、興味がある方は論文も併せてお読みください。
筆者は専門家ではないので、参考文献の解釈を間違えている可能性があることを踏まえた上で本記事をご一読いただけますと幸いです。
不老長寿の秘密





突然ですが、ノウキンさんは今何歳ですか?



本当に突然ですね(汗)
アラサーとだけ言っときます。



じゃあ、僕とそんなに変わらないですね。
僕もアラサーですよ。



デバ吉がアラサー!?
ハダカデバネズミの寿命って何年あるんですか?汗



ハダカデバネズミの平均寿命は約30年です。
飼育下では40年近く生きた個体もいるらしいですよ。



30年とか40年って…
マウスの10倍くらいあるじゃないですか!
真社会性の哺乳類の生物であることが注目され、研究対象として飼育され始めたハダカデバネズミ。
しかし、研究が進む過程で異常に寿命が長いことが判明し、その驚異的な生命力も研究者達に注目されました。
具体的には、ハダカデバネズミの平均寿命は約30年。
一方で、同じ齧歯目かつ大きさが比較的近いマウスやラットの寿命は約2〜3年。
ハダカデバネズミの寿命が郡を抜いて長いことがわかります。
しかも、ハダカデバネズミには加齢による生理機能の低下がほとんど起こりません。
言い換えると、死ぬまで老化の兆候がほとんど見られないのです。
一般的な生物からは考えられないブッ壊れのチート特性ですね。
ハダカデバネズミはまさに不老長寿の生物であり、人類の夢をすでに叶えていると言っても過言ではありません。



ハダカデバネズミには老化による衰えがほとんど見られません。
なので、不老長寿の生物と考えられているんですよ。



不老長寿!?
人類の夢を叶えちゃってるってこと!?



不死ではないので、それは言い過ぎな気がしますけどね。
最近ではハダカデバネズミの不老長寿のメカニズムも解明され始めているんですよ。



それはぜひ聞きたいです!
もしかしたらヒトに応用できたりするかも…?



ヒトに応用できるかはわかりませんが、ここではハダカデバネズミの不老長寿に関わるメカニズムを説明しますね。
そんなチート特性をもつハダカデバネズミですが、近年ではその不老長寿のメカニズムが解明され始めています。
本章では、細胞の老化について説明した後にハダカデバネズミの不老長寿のメカニズムを解説します。
細胞の老化
ハダカデバネズミの不老長寿について説明する前に、老化について前提を揃えたいと思います。
細胞レベルにおいて、老化とは「老化細胞が蓄積した状態」。
ここで言う『老化細胞』とは、細胞分裂が停止した細胞のこと。
つまり、これ以上増えることができない細胞です。




『老化細胞』は細胞分裂が停止した細胞です。
これが蓄積すると生体に悪影響を及ぼすと考えられています。



老化細胞は細胞分裂が停止した細胞…
細胞分裂ってなんで止まっちゃうんでしたっけ?汗



細胞分裂が停止する主な理由として考えられているのは、「細胞周期の停止」と「細胞分裂の限界」です。
細胞分裂が停止する理由としては、主に2つあげられます。
1つは、DNA損傷が蓄積したことによる細胞周期の停止。
こちらは細胞がむやみに増殖してガン化するのを防ぐこともあるので、負の側面ばかりではありません。
もう一つは、染色体末端の『テロメア』が限界まで短くなったことによる細胞分裂の限界。
こちらは何度も分裂した末に起こる現象なので、細胞の寿命とも言えます。
これらの理由で生じた老化細胞は、通常であれば免疫細胞が除去します。
しかし、年歳を重ねると免疫細胞の機能低下に伴って老化細胞を除去しきれなくなってきます。
除去されずに残った老化細胞は、炎症性のサイトカインなど周囲の細胞に悪影響を及ぼす物質を継続的に分泌。
それが広がることで生理機能の低下につながり、老化が進行してしまうと考えられています。



多くの生物では歳を取ると老化細胞を除去しきれなくなります。
老化細胞の除去が不老長寿の鍵ということですね。



年を取ると体調が不安定になるのは老化細胞が蓄積したせいですかね…
若い頃はそんなことはなかったんですけどね(泣)



それは免疫細胞の機能が低下して老化細胞を除去しにくくなっているのかもしれませんね。



免疫細胞の機能が低下(汗)
ハダカデバネズミはそうならないんですか?



ハダカデバネズミの場合は、免疫細胞を頼らずに老化細胞を除去するメカニズムが積極的に働いているんですよ。



そんな便利なメカニズムが…!
めっちゃ気になります!



次はそのメカニズムについて説明しますね。
不老長寿の秘訣は「幸せホルモン」
老化の原因の1つとして老化細胞の蓄積があることを説明しました。
多くの生物が歳を取るにつれて免疫細胞による老化細胞の除去が追いつかなくなり、老化が進行すると考えられています。
不老長寿であるハダカデバネズミはどのように老化細胞の蓄積を防いでいるのでしょうか?
その疑問が近年の研究で明らかになり、『セロトニン』という物質が関わっていることが判明しています。



ハダカデバネズミの不老長寿には『セロトニン』が関係しています。



あの「幸せホルモン」で有名なやつですか?
まさか幸福を感じると老化細胞が除去されるとでも?



その可能性もゼロではありませんね。
でも、もっと具体的なメカニズムが判明してますよ。
セロトニンは一般的に「幸せホルモン」として知られている物質。
この記事を読む読者の多くが一度はその名を耳にしたことがあるのではないでしょうか?
ヒトでは脳内で神経伝達物質として働いたり、腸の運動を調整しているセロトニン。
ヒトにおける存在比率は消化管の表面に約90%、脳に約10%と特定の部位に局在していると言われています。
しかし、ハダカデバネズミではより多くの細胞にセロトニンが蓄積。
ハダカデバネズミの細胞が老化細胞になると蓄積したセロトニンが『5-ヒドロキシインドール酢酸(5-HIAA)』に変換され、この過程で『過酸化水素(H2O2)』が発生します。
そして、ハダカデバネズミの生体内では、このH2O2 がトリガーとなって細胞死が誘発されることが判明しました。
この際に起こる細胞死は、細胞が自ら断片化する『アポトーシス』などのプログラム細胞死が中心です。
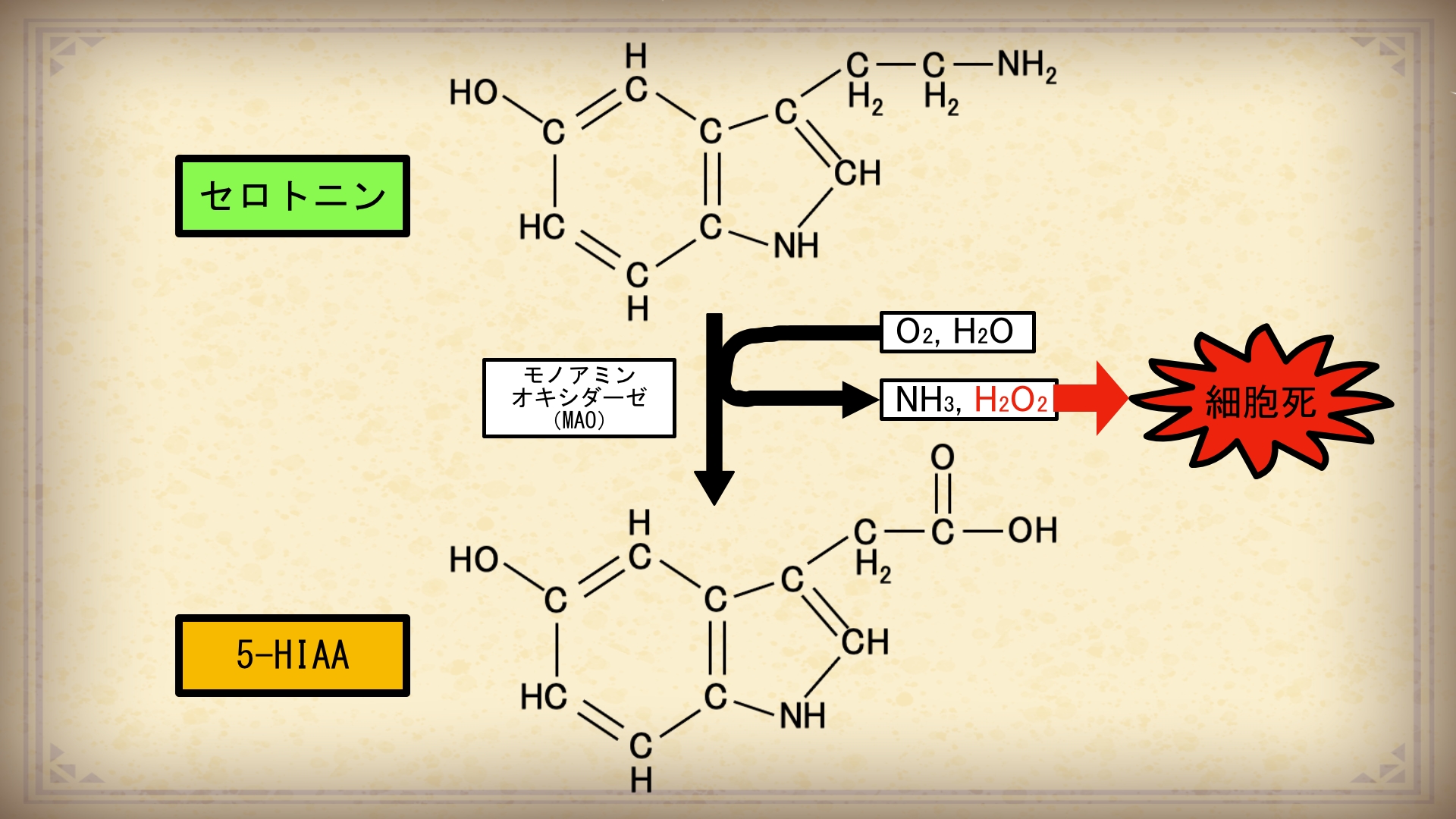




ハダカデバネズミの細胞が老化細胞になるとセロトニンが『5-HIAA』に変換されて、その過程で『H2O2』が発生します。
そのH2O2がトリガーとなって老化細胞が細胞死を起こすんです。



老化細胞がセロトニン代謝の過程で発生するH2O2に反応して自ら細胞死を起こすんですね!



まとめるとそんな感じですね。
このセロトニン由来の細胞死はH2O2に過剰反応するハダカデバネズミの細胞に特有であると考えられているんですよ。
セロトニン由来の細胞死はH2O2 に過剰反応するハダカデバネズミの細胞特有のメカニズムであると考えられています。
実際、研究で比較対象とされたヒトやマウスの細胞では確認されていません。
ヒトやマウスにおける老化細胞の除去は免疫細胞によるものが大半なので、加齢に伴って免疫細胞の機能が低下して老化細胞除去の効率が落ちます。
しかし、セロトニン由来の細胞死は免疫細胞を介さないため、加齢の影響はほとんどありません。
そのため、ハダカデバネズミは歳を取っても老化細胞が蓄積せず、老化の兆候がほとんど見られないと考えられています。
老化の兆候がなければ病気にもなりづらく、当然それに伴って寿命も伸びます。
つまり、このセロトニン由来の細胞死こそがハダカデバネズミの長寿の秘密というわけです。



セロトニン由来の細胞死はハダカデバネズミの細胞特有なんですね…
それだとヒトに応用するのは難しいか(汗)



ハダカデバネズミから不老薬を作るのは難しいでしょうね。
ですが、この研究を進めることで不老薬を作るヒントが得られる可能性はあるかもしれませんよ。



人類の夢に繋がる研究になるかもしれないのか…!
今後もハダカデバネズミの研究から目が離せませんね!
参考文献
Cellular senescence induction leads to progressive cell death via the INK4a-RB pathway in naked mole-rats
著者:Yoshimi Kawamura, Kaori Oka, Takashi Semba, Mayuko Takamori, Yuki Sugiura, Riyo Yamasaki, Yusuke Suzuki, Takeshi Chujo, Mari Nagase, Yuki Oiwa, Shusuke Fujioka, Sayuri Homma, Yuki Yamamura, Shingo Miyawaki, Minoru Narita, Takaichi Fukuda, Yusuke Sakai, Takatsugu Ishimoto, Kazuhito Tomizawa, Makoto Suematsu, Takuya Yamamoto, Hidemasa Bono, Hideyuki Okano, Kyoko Miura
掲載誌:The EMBO Journal(2023)
リンク:https://www.embopress.org/doi/full/10.15252/embj.2022111133
驚異的なガン化耐性


不老長寿のメカニズムだけでも十分に興味を惹かれるハダカデバネズミ。
しかし、ハダカデバネズミにはそれと同じくらい驚異的な特性があります。
その能力こそが、ガン化耐性。
過去にはハダカデバネズミを800匹飼育してもガンになった個体がいなかった例もあるそうです。
本章では、そんなハダカデバネズミの驚異的なガン化耐性について解説します。



不老長寿だけでなく、ガン化耐性まで!?
ちょっとチート過ぎませんか?



確かに普通の生物にはない特性ですね。
ハダカデバネズミのガン化耐性についてもいくつかのメカニズムが解明され始めているんですよ。



ガン化耐性のメカニズム!
めっちゃ気になります!



いくつかありますが、まずは『ヒアルロン酸』が関わるメカニズムを説明しますね。



また聞いたことのある物質だ…
ガン化耐性との関係性が全然想像できない(汗)
細胞増殖をコントロールする『ヒアルロン酸』
ハダカデバネズミの驚異的なガン化耐性に関係していることが判明したのが『ヒアルロン酸』。
ヒアルロン酸はヒトにも存在しており、特に皮膚では水分を保つことで乾燥を防ぐ役割を果たします。
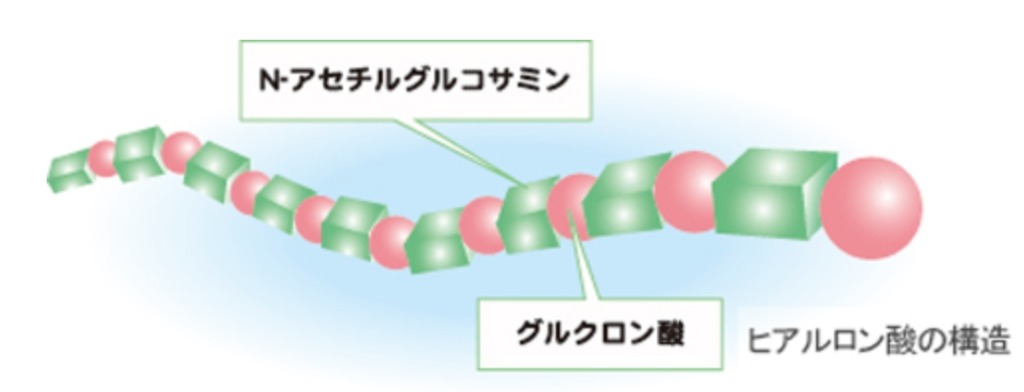

構造的には、『グルクロン酸』と『N-アセチルグルコサミン』という2種類の糖が直鎖上に交互に結合した重合体。
ヒアルロン酸はそれらが結合した数、言い換えると分子量によって区別されます。
分子量が小さいヒアルロン酸は『低分子ヒアルロン酸(LMW-HA)』、分子量が大きいヒアルロン酸は『高分子ヒアルロン酸(HMW-HA)』と呼ばれます。
HMW-HAの定義は分子量1,000 kDa(100万Da)以上で、ヒアルロン酸合成酵素によって生成。
一方で、LMW-HAはヒアルロン酸分解酵素などによってHMW-HAが分解されることで生成されます。



ヒアルロン酸は高分子量の『HMW-HA』と低分子量の『LMW-HA』に分けられます。



ヒアルロン酸にも種類があるんですね。
それぞれの分子量はどれくらいなんですか?



ヒトやマウスの場合、HMW-HAは100万Da以上、LMW-HAは数万Da以下と言われています。



タンパク質の多くが数万〜数十万Daと考えると、ヒアルロン酸はかなり大きな物質なんですね(汗)



ハダカデバネズミのヒアルロン酸の分子量はヒトやマウスよりさらに大きいですけどね。



さらに大きいの!?
ヒアルロン酸の分子量は生物毎に異なります。
ハダカデバネズミの場合、他の生物と比較してHMW-HAの分子量が大きいことが特徴です。
その大きさは、なんとヒトやマウスのヒアルロン酸の5倍以上。
ヒトやマウスのHMW-HAの分子量が約1,000 kDa(100万Da)なので、ハダカデバネズミのHMW-HAは5,000 kDa(500万Da)以上になると考えられます。





ハダカデバネズミのHMW-HAの分子量はヒトやマウスの5倍以上も大きいんですよ。



5倍以上!?
でも、それがガン化耐性とどう関係するんですか?汗



HMW-HAの分子量が大きいことによるガン化耐性への関与は現時点では判明していません。



判明してないんかい!



ただ、HMW-HAは細胞のガン化を抑制するメカニズムのトリガーになることがわかっているんですよ。
正常な細胞がDNA損傷などのエラーによって異常が起きると『ガン細胞』になることがあります。
ガン細胞は無秩序に増える性質があり、放置すると目視でも確認できる腫瘍を形成してしまいます。
このような無秩序な細胞増殖を抑制するメカニズムの1つに『Hippo経路』が存在。
Hippo経路はシグナル伝達経路であり、ヒアルロン酸はこのシグナル伝達をコントロールします。
ヒアルロン酸の多くは細胞外に存在しており、細胞膜に存在する『CD44』と結合。
CD44に結合したのがHMW-HAの場合、細胞内でHippo経路を活性化するシグナル伝達が開始します。
詳しい内容は割愛しますが、Hippo経路により細胞増殖は抑制する方向にコントロールされます。
細胞増殖が抑制されるということは、同時に細胞のガン化も抑制されるということ。
つまり、HMW-HAは細胞のガン化を抑制するトリガーになるということです。
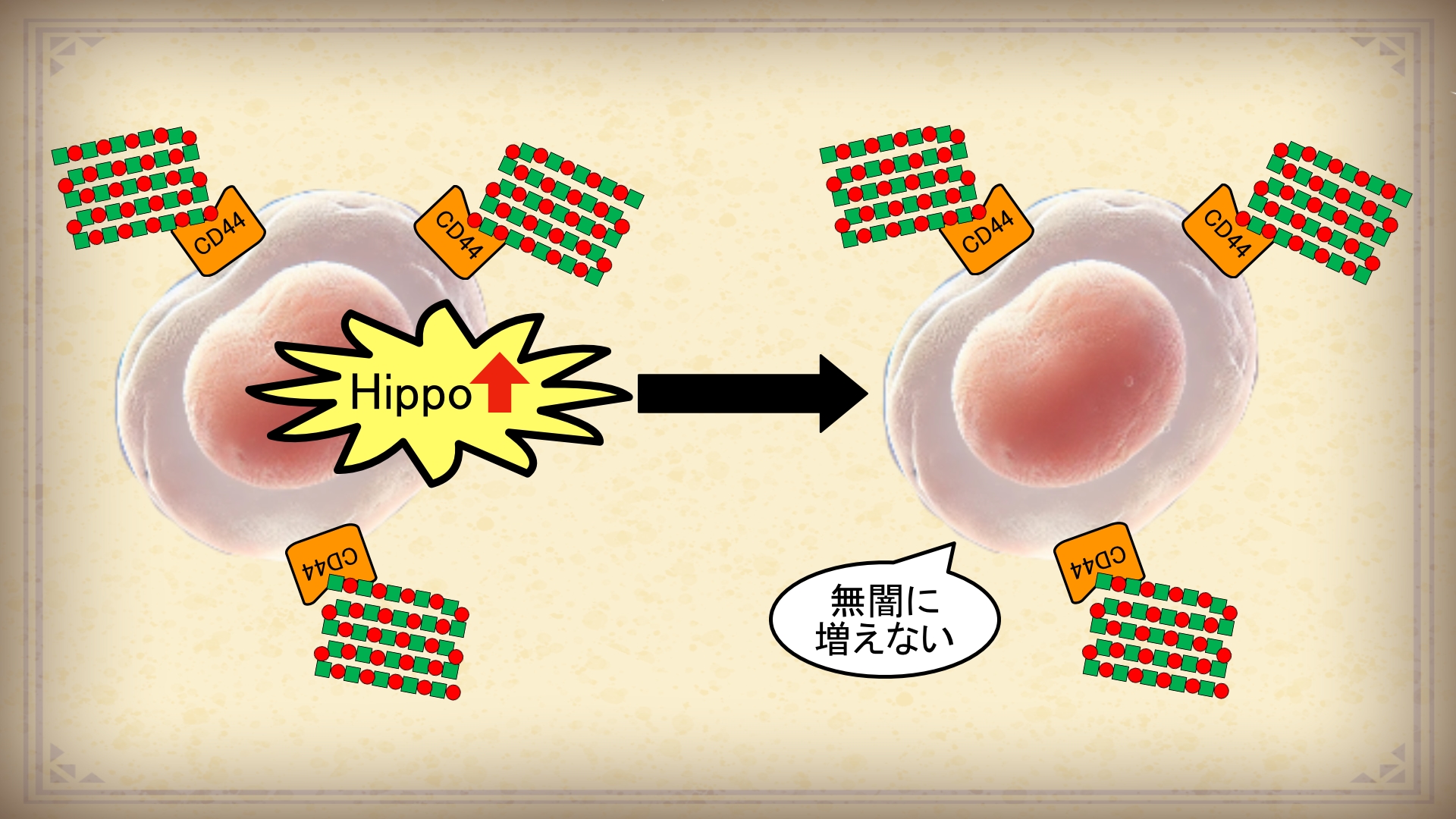




HMW-HAが細胞表面の『CD44』と結合して、細胞内の『Hippo経路』が活性化されることで細胞増殖が抑制されます。



細胞増殖が抑制されるということは、細胞のガン化も抑制されるってことですね!



そういうことです。
逆に、LMW-HAがCD44と結合した場合は細胞のガン化が促進されると考えられています。
一方で、CD44に結合したのがLMW-HAの場合、Hippo経路は活性化されません。
それどころか、HMW-HAとCD44の結合を阻害してしまいます。
つまり、LMW-HAは細胞増殖が促進する方向にコントロールするのです。
上記の原理によって、過剰なLMW-HAは細胞のガン化を促進すると考えられています。
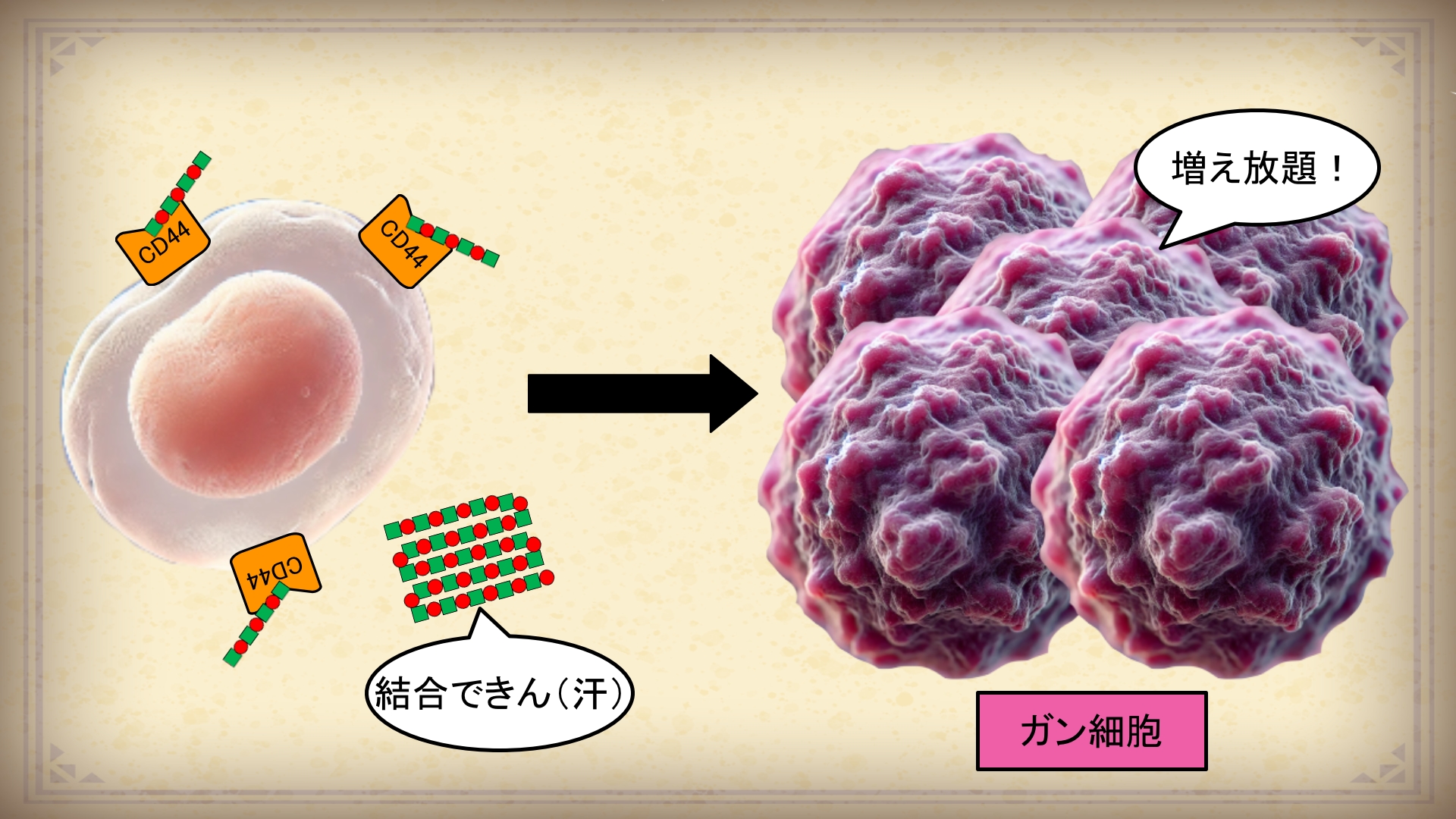




LMW-HAがCD44に結合してもHippo経路は促進されません。
しかも、HMW-HAとCD44の結合を阻害してしまうんです。



つまり、LMW-HAはHippo経路を抑制するってことですか?



そういうことですね。
Hippo経路が抑制されると、細胞増殖が抑制されなくなってガン化が促進されてしまうんです。



じゃあ、LMW-HAが大量に存在するとガンになりやすいってことか…



現時点では、そのように考えられますね。
ハダカデバネズミの生体内ではLMW-HAが過剰にならないようにヒアルロン酸の合成酵素や分解酵素に特徴があるんです。
分子量の異なるヒアルロン酸によってコントロールされるHippo経路。
このシグナル伝達経路は多くの生物に保存されており、ハダカデバネズミにも共通しています。
他生物と比較して高分子のHMW-HAをもつハダカデバネズミですが、これは『Has2』などのヒアルロン酸合成酵素の発現量が高いことに由来していると考えられています。
その上、ハダカデバネズミのヒアルロン酸分解酵素は機能不全だったり発現量が低いことも判明。
つまり、ハダカデバネズミの生体内ではHMW-HAが分解されにくくLMW-HAが生成されにくいのです。
これらの条件により、他生物に比べてハダカデバネズミの細胞ではHippo経路が活性化されやすく、ガン化耐性を得ていると考えられます。
実際、ヒアルロン酸を分解する酵素を発現させたハダカデバネズミにおいて細胞がガン化して腫瘍を形成したという結果が得られています。



ハダカデバネズミの生体内ではヒアルロン酸合成酵素の発現量が多い一方でヒアルロン酸分解酵素の発現量が少なくなっているんですよ。



つまり、ハダカデバネズミの生体内ではHMW-HAが存在しやすい状況なんですね!



そういうことですね。
恐らく、ハダカデバネズミのHMW-HAが他の生物よりも高分子なのは、その環境の副産物なのでしょう。



ヒアルロン酸合成酵素が強く働いているなら、そう考えるのが自然ですよね。



ちなみに、HMW-HAは粘性がとても高いそうです。
おかげでハダカデバネズミの細胞はとてもネバネバしてるんだとか。



実験や後片付けが大変そう(汗)



実際、大変だったそうですよ。
でも、このネバネバした物質を調べてみたらガン化耐性に関わっていたのだから驚きですよね。



それを調べなかったら、この発見はなかったかもしれないですからね!
ひょんなことから大発見につながるのは研究の醍醐味です(笑)
参考文献
High-molecular-mass hyaluronan mediates the cancer resistance of the naked mole rat
著者:Xiao Tian, Jorge Azpurua, Christopher Hine, Amita Vaidya, Max Myakishev-Rempel, Julia Ablaeva, Zhiyong Mao, Eviatar Nevo, Vera Gorbunova, Andrei Seluanov
掲載誌:Nature(2013)
リンク:https://www.nature.com/articles/nature12234(本文有料)
High-Molecular-Weight Hyaluronan Is a Hippo Pathway Ligand Directing Cell Density-Dependent Growth Inhibition via PAR1b
著者:Takuya Ooki, Naoko Murata-Kamiya, Atsushi Takahashi-Kanemitsu, Weida Wu, Masanori Hatakeyama
掲載誌:Developmental Cell(2019)
ガン化に対する二重の防御機構
高分子ヒアルロン酸が存在することで細胞のガン化を抑制できるハダカデバネズミ。
さらに、細胞がガン化しても発生初期の段階でガン細胞を除去するメカニズムが存在します。
そのメカニズムに関与している遺伝子が『ARF』。
ARF はガン化を誘導するストレスに反応して転写が促進(活性化)される『ガン抑制遺伝子』です。
また、ARF はガン化に対する最初の防御機構に関わる因子の1つでもあり、この防御機構によってガン細胞は発生初期に抑制または除去されます。



次に紹介するガン化耐性のメカニズムには、ガン抑制遺伝子『ARF』が関わっています。



流石にそれは驚きませんね(汗)
ガン抑制遺伝子がガン化耐性に関わるのは当然なのでは?



確かに、ARF は他の生物でもガン化耐性に関わっています。
ただし、ハダカデバネズミの場合はARF が抑制された場合に対応するメカニズムもあるんですよ。



ガン細胞に対してプランB的なメカニズムがあるってこと!?
ARF はハダカデバネズミ特有の遺伝子ではなく、他の生物においてもガン抑制遺伝子として働いています。
そのため、ARF の活性化によるガン化耐性はハダカデバネズミ特有ではなく、珍しくはありません。
しかし、変異が入るなどしてARF が抑制された細胞はガン化のリスクが段違いに上昇。
多くの生物ではARF が抑制された細胞を除去する手段がなく、そのまま放置してガン化してしまいます。
一方で、ハダカデバネズミにはARF が抑制された細胞を除去する独自のメカニズムが存在します。
そのメカニズムとは、細胞の老化促進。
つまり、ハダカデバネズミの細胞はARF が抑制されると細胞増殖が停止して老化細胞になってしまうのです。
このハダカデバネズミ特有のメカニズムは『ARF抑制時細胞老化(ASIS)』と呼ばれています。
『老化』という単語を聞いて、勘の良い読者は気づいたかもしれませんね。
そう、ASISによって老化促進された細胞は上述したセロトニン由来の細胞死によって除去されることが予想できます。
「ASIS→セロトニン由来の細胞死」の流れは論文を確認したわけではないので筆者の予想にはなりますが、全く関係がないとは考えにくいです。
つまり、ハダカデバネズミの細胞ではガン化に対して以下のような二重の防御機構があると考えられます。
- ガン化誘導ストレスに対するガン抑制遺伝子ARF の活性化(通常時)
- ASISによる細胞老化→セロトニン由来の細胞死(ARF 抑制時)
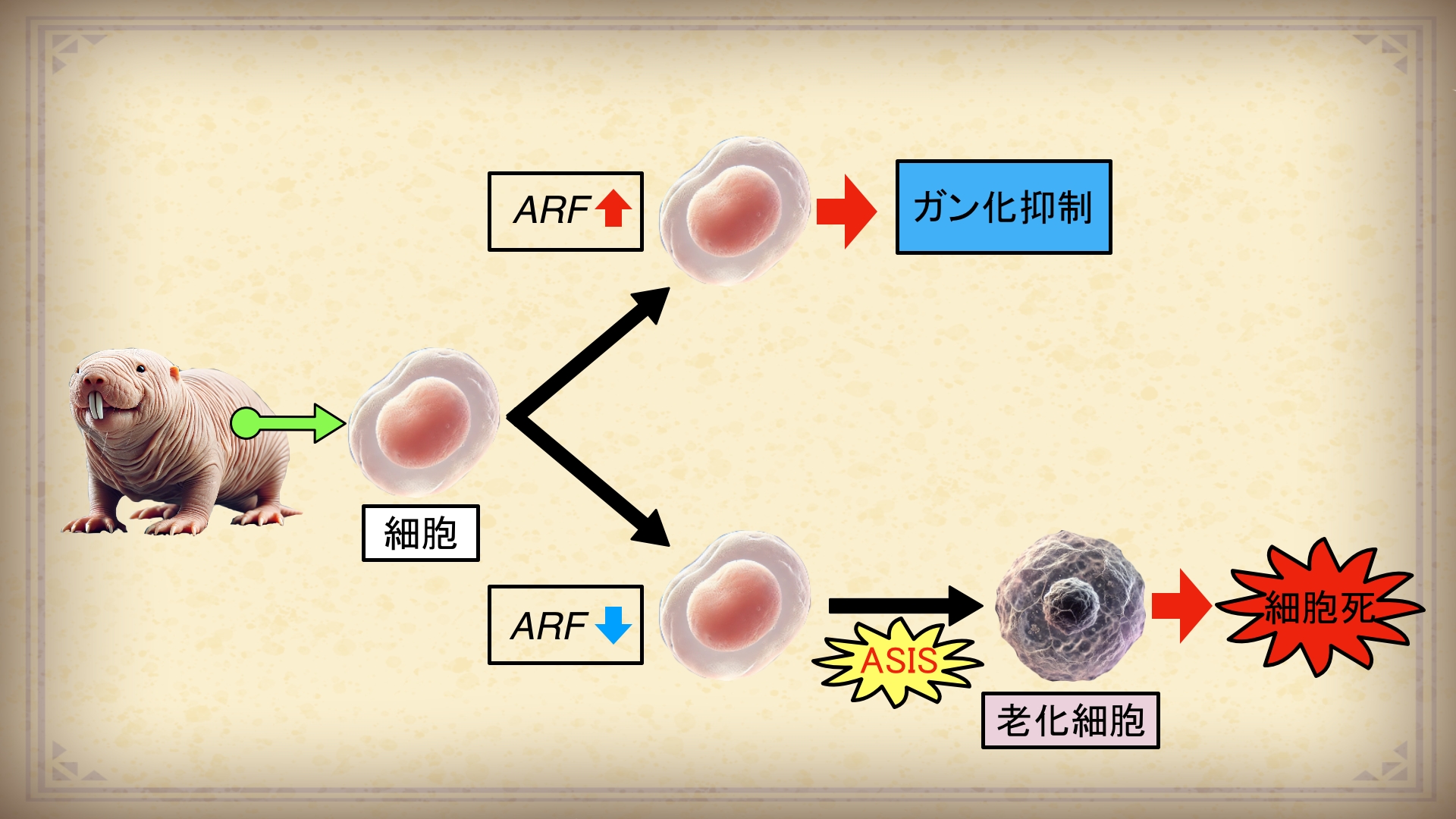




ARF が抑制された細胞は老化細胞になってしまうんです。
このメカニズムは『ASIS』と呼ばれています。



細胞が老化するメカニズム…
老化細胞になったということは…



セロトニン由来の細胞死が起こることが予想されますね。



言われてしまった(泣)



すいません、調子に乗ってしまいました。
要するに、ハダカデバネズミにはARF の活性化とASISというガン化に対する二重の防御機構があるんです。



HMW-HAによるガン化耐性もあるから、ハダカデバネズミがガンになることはそうそうないってことか…



ハダカデバネズミのガン化耐性のメカニズムの説明は以上です。
難しい話が続いたので、今回はここまでにしましょう。
参考文献
Tumour resistance in induced pluripotent stem cells derived from naked mole-rats
著者:Shingo Miyawaki, Yoshimi Kawamura, Yuki Oiwa, Atsushi Shimizu, Tsuyoshi Hachiya, Hidemasa Bono, Ikuko Koya, Yohei Okada, Tokuhiro Kimura, Yoshihiro Tsuchiya, Sadafumi Suzuki, Nobuyuki Onishi, Naoko Kuzumaki, Yumi Matsuzaki, Minoru Narita, Eiji Ikeda, Kazuo Okanoya, Ken-ichiro Seino, Hideyuki Saya, Hideyuki Okano, Kyoko Miura
掲載誌: Nature communications(2016)
エピローグ



不老長寿やらガン化耐性やらハダカデバネズミってとんでもなく凄い生物だったんですね…



そう思ってもらえたなら、頑張って説明した甲斐がありました。



ただ、内容が難しいから復習するのも大変なんですよね(汗)
論文を読むのも時間がかかりますし…



それなら前回紹介した本で復習したらどうですか?
不老長寿やガン化耐性といった驚異的な特性をもつハダカデバネズミ。
人類にとって夢のような特性をもつと知り、ハダカデバネズミにより興味をもっていただけたかと思います。
各章毎に参考文献である論文のURLを載せていますが、それをしっかり読み込むには相応の労力が必要。
論文を読むのはまだ厳しいという方には、以下の書籍がオススメです。
ハダカデバネズミの写真やイラストがカラーで見やすく、本記事で紹介できなかった内容も書かれています。
2020年発売のため、それ以降に発表されたセロトニン由来の細胞死については載っていません。
しかし、それ以外については研究の背景も踏まえて書かれていますので、気になる方はぜひご一読ください。



確かに、デバ吉にオススメされた本で復習するのもありかも。



2020年発売の本なので、セロトニン由来の細胞死について載ってないことだけは注意してくださいね。



わかりました!
その内容だけは論文を読むようにします!



今回は難しい内容でしたから、しっかり復習してくださいね。
では、僕は業務に戻ります。



了解です!
デバ吉が昼寝してる間にしっかり勉強しますね!



ふとん係の仕事はただ昼寝するだけじゃないと説明したはずですが…
ノウキンさんの今後の成長に期待しましょう。
本記事はこれで終わりです。
最後までお読みいただき、ありがとうございました!


